在金飛鷹的日常輔導過程中我們發現,很多客戶在谘詢時最關注的兩個點,無非就是注冊費用及時長。那麼今天我們就來分享一下,注冊申報一個醫療器械產品到底需要多長時間?
具體來說,第三類醫械產品的注冊申報時間是要長於第二類醫療器械的,以下為國家藥監局器審中心發布的法定時限表:
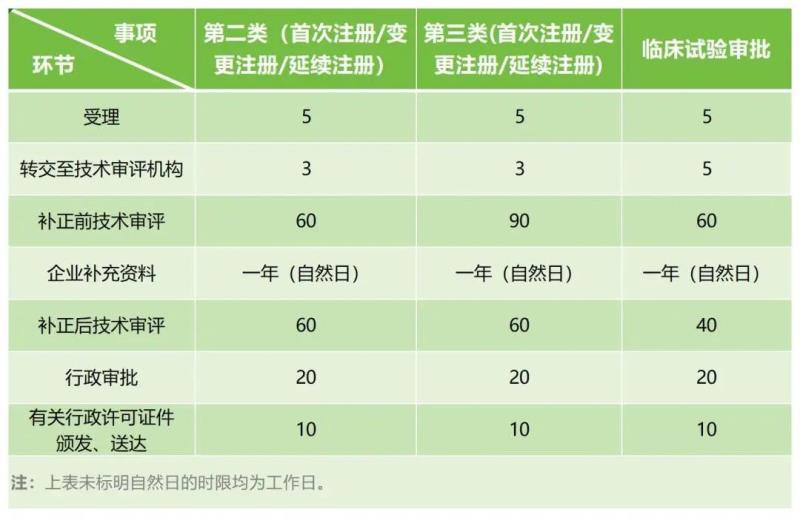
但是,如今很多省份都縮減了審評時限,比如,廣東省首次注冊審評時限由法定60個工作日壓縮至40個工作日,補正後技術審評時限由法定60個工作日壓縮至30個工作日,行政審批時限由法定20個工作日壓縮至10個工作日。還有江蘇、湖南等其他省份的審評時間,可點擊查看右側鏈接查看→多省審評時限彙總
根據器審中心統計的2022年審評工作總體用時,按管理類別看,二類產品注冊審評總體平均用時為72個工作日,三類產品注冊為99個工作日;按申請事項看,產品首次注冊審評總體平均用時為95個工作日,變更注冊為64個工作日,延續注冊為39個工作日。
最後需注意的是,以下時間不計入上述相關工作時限:
(一)申請人補充資料、核查後整改等所占用的時間;
(二)因申請人原因延遲核查的時間;
(三)外聘專家谘詢、召開專家谘詢會、藥械組合產品需要與藥品審評機構聯合審評的時間;
(四)根據規定中止審評審批程序的,中止審評審批程序期間所占用的時間;
(五)質量管理體係核查所占用的時間。
醫療器械注冊谘詢認準金飛鷹
深圳:0755-86194173
廣州:020 - 82177679
湖南:0731-22881823
四川:028 - 68214295


