10月11日,國家藥監局器審中心發布《醫療器械人因設計注冊審查指導原則(征求意見稿)》,並宣布第二次(第一次為2020年5月)公開征求意見。
意見反饋時間:2023年10月30日前
意見反饋郵箱:pengliang@cmde.org.cn
我們將其中部分重點內容摘錄如下:
本指導原則適用於第二類、第三類醫療器械人因設計的注冊申報,不適用於體外診斷試劑。注冊申請人可參照本指導原則要求開展全部醫療器械的人因設計工作。
從醫療器械安全有效性評價角度出發,本指導原則所述人因設計是指綜合運用關於人類的解剖、生理、心理、行為、文化等方麵能力與限製的人因工程知識來設計開發醫療器械,以增強醫療器械的可用性。人因工程亦稱可用性工程、人機工效學/人體工程學,人因工程知識包括但不限於身體、感知、認知、行動等方麵知識。
可用性(Usability)是指預期用戶在預期使用場景下正常使用醫療器械時,保證醫療器械安全有效使用的用戶接口易用特性。易用特性包括但不限於易讀性、易理解性、易學習性、易記憶性、易操作性、用戶差錯防禦性等特性。本指導原則所述可用性僅限於與醫療器械安全有效使用相關的用戶接口特性,注冊申請人可參考本指導原則設計開發其他用戶接口特性,如用戶滿意度、使用意願等。
用戶、使用場景和用戶接口是人因設計的三個核心要素。
1.用戶
用戶是指注冊申請人所規定的醫療器械操作人員,如醫務、患者、家庭護理、清潔、運輸、安裝、維修、處置等人員。用戶通常可分為多個用戶組,用戶組即具有某一用戶特征的用戶人群。用戶特征用於反映用戶組自身在解剖、生理、心理、行為、文化等方麵的獨特性,包括但不限於用戶人群的人口統計學(如性別、年齡)、人體測量學(如身高、體重、力量)、能力(如感知、認知、行動)、文化(如社會關係、職業傳統、語言)等方麵特征以及知識水平、職業技能、工作經驗、培訓程度等方麵要求。
用戶若為或含有兒童、老人、孕婦以及殘障人士等特殊人群,由於其用戶特征與普通人群存在較大差異,故需考慮可及性要求。同時,亦需綜合考慮用戶在健康、疾病、服藥等不同狀態下的能力及其限製,必要時明確用戶限製。
注冊申請人需根據醫療器械用戶特征情況規定用戶/用戶組要求。本指導原則重點關注醫務、患者、家庭護理等操作醫療器械實現其預期用途的用戶/用戶組,包括醫療器械消毒滅菌操作人員,暫不考慮清潔、運輸、安裝、維修、處置等操作人員,待時機成熟時納入考量。不過注冊申請人需考慮全部用戶/用戶組的人因設計要求。
2.使用場景
如圖1所示,使用場景是指注冊申請人所規定的醫療器械實際使用的場景因素,包括使用環境和操作任務。使用環境是指用戶操作醫療器械的實際環境,又可分為使用場所、環境條件,其中使用場所包括門診室、急診室、手術室、病房、救護車、家庭、公共場所等情況,環境條件包括空間、照明、溫度、濕度、氣壓、潔淨度、噪聲、振動、輻射等情況。操作任務是指用戶操作醫療器械以實現特定目標的行動或行動序列,本指導原則重點關注醫療活動相關操作任務,暫不考慮清潔、運輸、安裝、維修、處置等操作任務(醫療器械安全標準若有相應要求除外),待時機成熟時納入考量。不過注冊申請人需考慮全部操作任務的人因設計要求。
操作任務從不同角度出發有不同分類方法。從風險角度可分為關鍵任務和非關鍵任務,關鍵任務是指用戶行動或行動缺失可能導致嚴重傷害或死亡的操作任務,反之即為非關鍵任務。從操作緊迫性角度可分為緊急任務和非緊急任務,緊急任務是指需要用戶立刻執行的操作任務,反之即為非緊急任務。從操作頻率角度可分為常用任務和非常用任務,常用任務是指用戶經常使用的操作任務,反之即為非常用任務。關鍵任務、緊急任務和常用任務相互關係如下:緊急任務通常屬於關鍵任務,常用任務與關鍵任務、緊急任務存在交集,某一特定操作任務可以同時為上述二種或三種任務。本指導原則關注醫療器械潛在使用風險,故以關鍵任務作為操作任務分類主線,兼顧緊急任務和常用任務,即重點關注兼為緊急任務、常用任務的關鍵任務。

注冊申請人需規定醫療器械關於使用場所、環境條件和操作任務的要求,並識別關鍵任務及其風險,特別是兼為緊急任務、常用任務的關鍵任務。
3.用戶接口
用戶接口(又稱用戶界麵)是指用戶與醫療器械人機交互的全部對象及方式,包括醫療器械的形狀尺寸重量、顯示反饋、連接組裝、操作控製、說明書與標簽、包裝、用戶培訓材料等。
注冊申請人需以操作任務為導向,結合用戶、使用場所、環境條件進行用戶接口設計。
1.醫療器械使用情況
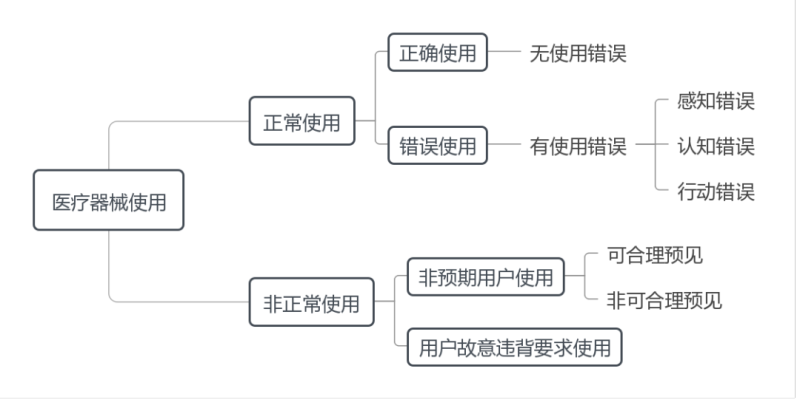
如圖2所示,醫療器械使用情況可分為正常使用和非正常使用,其中正常使用是指用戶按照說明書要求及常識慣例操作醫療器械,反之即為非正常使用。
正常使用從使用結果角度可分為正確使用和錯誤使用,其中正確使用是指沒有錯誤使用的正常使用,其產生的風險均可接受;錯誤使用是指用戶行動或行動缺失導致異於注冊申請人或用戶所預期的醫療器械響應,其可能降低醫療器械的有效性或者產生不可接受的風險,導致患者、用戶或相關人員受到傷害或死亡。
使用錯誤是指可能導致錯誤使用的潛在根源,可分為感知錯誤、認知錯誤和行動錯誤。其中,感知錯誤是指用戶對視覺、聽覺、觸覺等信息感知失效所致的使用錯誤,如看錯輸出結果單位、未聽到報警聲音等;認知錯誤是指用戶對知識、規則、信息存在記憶、理解等認知失效所致的使用錯誤,如漏記手術操作步驟、誤解符號含義等;行動錯誤是指用戶操作失誤、不當等行動失效所致的使用錯誤,如按錯控製按鈕、按壓力度不夠而未激活等。
非正常使用包括非預期用戶使用、用戶故意違背要求使用或二者兼而有之等情況,其中非預期用戶使用可分為可合理預見、非可合理預見兩種情況。
雖然注冊申請人可參考本指導原則識別醫療器械非正常使用的風險,但本指導原則僅限於醫療器械正常使用的風險考量,同時從風險管理角度考慮可合理預見非預期用戶使用的風險,如供成人使用的家用醫療器械需考慮兒童使用風險。
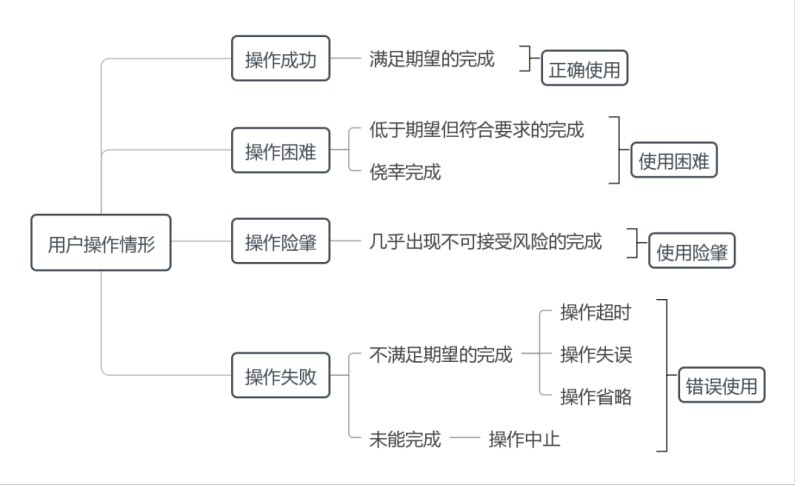
醫療器械在使用階段需要人機交互方能實現其預期用途,人機交互核心問題在於用戶接口設計能否保證醫療器械使用的安全有效性。因此本指導原則聚焦於醫療器械的用戶接口設計問題,從醫療器械設計開發角度考慮人因設計相關要求。
醫療器械人因設計是醫療器械安全有效性的重要組成部分,需基於醫療器械的預期用途、使用場景、核心功能分析並控製醫療器械使用風險,結合用戶和使用場景開展用戶接口設計,不能脫離安全有效性孤立進行人因設計。
醫療器械人因設計若存在問題將不利於人機交互,可能產生使用風險,影響到醫療器械使用的安全有效性。同時,醫療器械不良事件和召回數據也表明醫療器械使用問題較為突出,使用風險不容忽視,主要原因在於醫療器械人因設計存在問題。因此,醫療器械需要加強人因設計,特別是在采用全新使用方式、學習曲線長、非專業用戶使用、生命支持、藥械聯用、急救、家用、適用於脆弱人群(如兒童、孕婦、老人)等情況下。
考慮到使用風險所致傷害發生概率在執行層麵難以統計,故將醫療器械使用風險按傷害嚴重度分為高、中、低三個級別,分別指錯誤使用可能導致嚴重傷害或死亡、可能導致輕微傷害、不可能導致傷害。根據關鍵任務的定義,高使用風險醫療器械含有關鍵任務,中、低使用風險醫療器械不含關鍵任務。
醫療器械使用風險級別可通過風險管理進行判定,原因在於醫療器械使用風險是醫療器械風險管理的重要組成部分。風險管理所定義的風險等級與本指導原則所述醫療器械使用風險級別可以不同,不過二者存在對應關係,因此可根據風險管理所定義的風險等級來判定醫療器械使用風險級別,但需在采取風險控製措施之前進行判定。
值得注意的是,高使用風險醫療器械屬於高風險醫療器械(可能導致嚴重傷害或死亡的醫療器械),但高風險醫療器械並非都是高使用風險醫療器械,若其采用全新使用方式、學習曲線長、非專業用戶使用通常屬於高使用風險醫療器械,即高風險醫療器械若含有關鍵任務則為高使用風險醫療器械。
同時,醫療器械使用風險級別還可通過同類醫療器械上市後不良事件和召回情況進行判定,即同類醫療器械上市後發生與用戶使用和/或用戶接口設計相關的嚴重不良事件或一級召回屬於高使用風險,發生不良事件或二級召回屬於中度使用風險,未發生不良事件且僅發生三級召回或無召回屬於低使用風險。
醫療器械人因設計需結合用戶、使用場景和用戶接口開展風險管理,采用失效模式與效應分析(FMEA)、故障樹分析(FTA)等風險分析方法及其衍生方法,通過用戶接口設計(首選)、防護措施、安全信息等風險控製措施將醫療器械使用風險降至可接受水平,必要時開展用戶培訓,特別是對高使用風險醫療器械。
考慮到行業實際情況,高使用風險醫療器械當前僅限於部分第三類醫療器械,詳見附件1;未在醫療器械分類目錄的全新第三類產品可根據上述方法判定其使用風險級別。
醫療器械全生命周期均需考慮人因設計要求。上市前將人因設計納入醫療器械設計開發和風險管理過程,識別可預見的使用風險並將其降至可接受水平。上市後結合醫療器械使用問題(含不良事件和召回,下同),識別前期未預見的使用風險並改進人因設計,進一步提高醫療器械使用的安全有效性。
醫療器械人因設計是一個反複迭代、逐步細化的過程,注冊申請人需在質量管理體係設計開發程序的框架下開展人因設計可追溯性分析,即識別、追蹤並分析人因設計的輸入、輸出、驗證、確認、風險管理之間的關係,人因設計更改亦需開展人因設計可追溯性分析。
綜合考慮行業發展水平和使用風險分級管理導向,醫療器械使用風險級別不同,其人因設計的生命周期質控要求和注冊申報資料要求亦不同。注冊申請人需基於風險管理,結合同類醫療器械上市後不良事件和召回情況,依據風險從高原則綜合判定醫療器械使用風險級別,並采取與之相適應的生命周期質控措施:高使用風險醫療器械原則上需開展完整人因設計生命周期質控工作,中、低使用風險醫療器械可基於風險管理過程開展人因設計生命周期質控工作。
信息來源:國家藥監局器審中心
排版整理:金飛鷹藥械
醫療器械注冊谘詢認準金飛鷹
深圳:0755-86194173
廣州:020 - 82177679
湖南:0731-22881823
四川:028 - 68214295


