
近日,安徽省藥監局發布通告稱,自2024年1月1日起,對安徽省第二類有源醫療器械首次注冊項目實行立卷審查工作,有關事項具體如下:
一、立卷審查適用於第二類有源醫療器械首次注冊申請事項。
二、安徽省藥品審評查驗中心在受理環節按照立卷審查要求,審查相應申請的申報資料,並對申報資料的完整性、合規性、一致性進行判斷。立卷審查不對產品安全性、有效性評價的合理性、充分性進行分析,不對產品風險受益比進行判定。
三、申請人在準備注冊申報資料時,可依據《安徽省第二類有源醫療器械首次注冊立卷審查要求(試行)》進行自查,申報時不需要提交自查表。
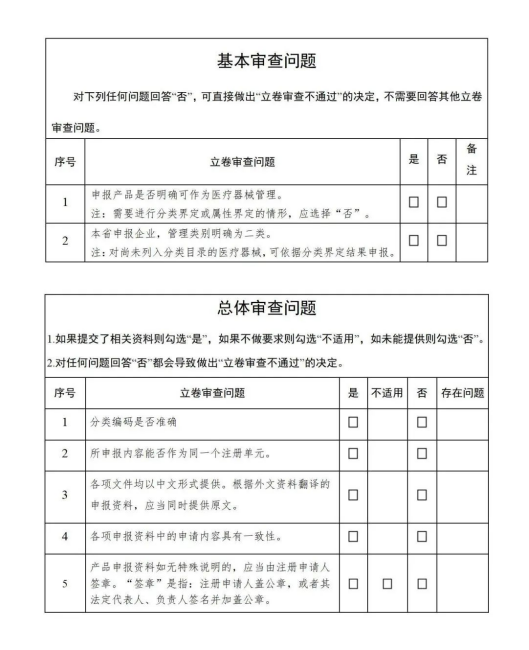
↑ 安徽省藥監局立卷審查基本審查問題&總體審查問題
以上僅對通告正文內容進行轉載,如需查看《安徽省第二類有源醫療器械首次注冊立卷審查要求(試行)》全文,可添加文末小編微信或點擊“閱讀原文”。
信息來源:安徽省藥監局
排版整理:金飛鷹藥械
醫療器械注冊谘詢認準金飛鷹
深圳:0755-86194173
廣州:020 - 82177679
湖南:0731-22881823
四川:028 - 68214295


